Влияние кефира на микробиом ротовой полости и кишечника человека

Оригинал статьи: Black EG, Bugarcic A, Lauche R, El-Omar E, El-Assaad F. The Effects of Kefir on the Human Oral and Gut Microbiome. Nutrients. 2025 Dec 11;17(24):3861.
Дисклеймер: переводные статьи размещаются на сайте FPA с целью расширения кругозора. Мнение авторов статей может не совпадать с позицией FPA.
Кефир — ферментированный пробиотический напиток, изготовленный из молока или из воды и растительных ингредиентов — набирает популярность в качестве пищевой добавки. Появившийся в Кавказских горах более 3000 лет назад, кефир считается полезным для здоровья благодаря своей способности изменять состав микробиологических ниш в организме человека. Эти микробиологические ниши называются микробиомами и включают совокупность микроорганизмов, их геномов и окружающей их среды. Современная коммерциализация кефира обусловила необходимость проведения высококачественных исследований, посвященных его влиянию на микробиом человека и связанные с этим последствия для здоровья. Однако в настоящее время научные данные, подтверждающие влияние потребления кефира на микробиом полости рта и кишечника человека, очень ограничены.
Прежде чем кефир можно будет рекомендовать для лечения заболеваний, связанных с микрофлорой полости рта и кишечника или метаболическим здоровьем, необходимы высококачественные клинические испытания на людях для подтверждения его безопасности и эффективности. Цель данного обзора научной литературы — критически проанализировать недавние исследования, посвященные влиянию потребления кефира на микробиом полости рта и кишечника, а также его потенциальное значение для здоровья человека. Изучая влияние кефира на эти взаимосвязанные микробные экосистемы, мы можем лучше понять его потенциал и ограничения применения в качестве функционального продукта питания для улучшения общего здоровья.
Введение
Термин «микробиом» впервые ввели в 1988 году Whipps с соавторами для описания совокупности микроорганизмов, обитающих в почве [1]. С тех пор значение этого термина расширилось; теперь оно включает в себя совокупности микроорганизмов, имеющих решающее значение для поддержания здоровья человека, и описывает как живые микроорганизмы в определенной экологической нише, так и их геномы. Микробиом кишечника обычно считается наиболее важным из микробиомов человека, учитывая его влияние на состояние метаболизма, иммунной системы, хронические заболевания, а также его сложную связь с различными органами и системами органов [2,3].
Микробиом кишечника, как правило, отличается широтой и разнообразием, включая до 100 триллионов микробов, относящихся к сотням и тысячам видов [4,5]. Это резко контрастирует с микробиомом полости рта — другой нишей в организме человека, которая оказывает большое влияние на здоровье. Хотя в ротовой полости было зарегистрировано более 700 таксонов микробов, их количество составляет всего 50–100 миллиардов, что намного меньше, чем в кишечнике [6]. Тем не менее, микробиом полости рта остается важным фактором, влияющим на здоровье человека, вследствие своей роли в пищеварительных и метаболических функциях, а также широкой связи с общим здоровьем [6].
Пробиотики употребляются во всем мире на протяжении тысячелетий и, как считается, способствуют улучшению здоровья, изменяя баланс микробиоты в определенной нише. Большинство пробиотических продуктов действуют в основном на кишечник, поставляя живые микроорганизмы, которые конкурируют с патогенными бактериями за питательные вещества и места прикрепления, вырабатывая антимикробные вещества, такие как бактериоцины и органические кислоты [7,8,9]. Кроме того, взаимодействуя с иммунной системой человека, эти микроорганизмы могут уменьшать локальное и системное воспаление и поддерживать целостность кишечного барьера [10,11,12].
Пробиотики естественным образом присутствуют в таких продуктах, как йогурт, квашеная (ферментированная) капуста, кимчи (ферментированная смесь овощей), но также доступны в виде пищевых добавок в форме капсул или порошка. Способность пробиотиков влиять на микробиологические ниши в организме человека делает их ценным инструментом для улучшения общего здоровья и профилактики заболеваний [13,14].
Кефир — это пробиотический молочный напиток, который появился в горах Кавказа более 3000 лет назад [15]. Его производят с использованием т. наз. кефирных зерен, которые представляют собой сложные симбиотические сообщества молочнокислых бактерий, уксуснокислых бактерий и дрожжей, встроенных в полисахаридную матрицу. Зерна добавляют в молоко, обычно коровье, что запускает процесс ферментации, в результате которого молоко становится густым и слегка кислым. В коммерческом производстве (рис. 1) молоко засевают кефирными зернами в соотношении от 1:30 до 1:50, а затем смесь оставляют ферментироваться до 24 часов при комнатной температуре [16,17].
В конце кефирные зерна отцеживают; оставшуюся жидкость можно сразу же употреблять или хранить при низких температурах для дальнейшего потребления [17,18]. Кефир можно также приготовить из козьего и овечьего молока или из веганских альтернатив, таких как соевое молоко и вода [19,20]. С расширением рынка коммерческого кефира расширились и возможности выбора низколактозных и веганских альтернатив, что позволяет людям с особыми диетическими потребностями употреблять этот напиток. Однако точный микробиологический состав кефирных напитков и, следовательно, их польза для здоровья могут в значительной степени зависеть от жидкого субстрата, используемого во время ферментации [19].
 Рисунок 1. Упрощенная схема коммерческого производства кефира. Кефирные зерна добавляются в молоко или напиток на водной/растительной основе в соотношении 1:30‒1:50; смесь подвергается ферментации при комнатной температуре. Через 24 часа зерна отцеживают, оставшийся напиток употребляют сразу или хранят для последующего потребления. По El-Assaad, F. (2025).
Рисунок 1. Упрощенная схема коммерческого производства кефира. Кефирные зерна добавляются в молоко или напиток на водной/растительной основе в соотношении 1:30‒1:50; смесь подвергается ферментации при комнатной температуре. Через 24 часа зерна отцеживают, оставшийся напиток употребляют сразу или хранят для последующего потребления. По El-Assaad, F. (2025).
Важным моментом, который необходимо учитывать при исследовании кефира, является его внутренняя неоднородность. Состав кефира значительно варьируется в зависимости от множества факторов, включая микробиологический профиль закваски, время ферментации, температуру ферментации [21,22,23,24]. Эти производственные переменные могут существенно влиять на конечный состав и относительную численность микроорганизмов, присутствующих в напитке, а также на концентрацию биологически активных метаболитов, образующихся в ходе ферментации.
Следовательно, конкретное действие на здоровье, наблюдаемое в одном исследовании, может быть несопоставимо напрямую с действием, наблюдаемом в другом, поскольку разные препараты кефира могут оказывать различное воздействие на микробиом. По этой причине данные об изменениях микробиома кишечника и полости рта после употребления кефира могут значительно различаться [25,26].
В микробиологическом составе кефира преобладают молочнокислые бактерии (МКБ), которые составляют 60–83% всей микробиологической популяции [27,28,29,30] (рис. 2). МКБ играют важную роль в ферментации молочных субстратов, метаболизируя лактозу и вырабатывая молочную кислоту. В ходе этого процесса МКБ также производят углекислый газ, ацетальдегид, бактериоцины, кателицидин и перекись водорода, которые, как было доказано, ослабляют и/или уничтожают распространенные кишечные патогены [31,32]. Одними из наиболее распространенных МКБ, присутствующих в кефире, являются Lentilactobacillus kefiri, Lactococcus lactis и Leuconostoc mesenteroides [33,34]. L. kefiri и L. mesenteroides выживают при прохождении через кишечник и прилипают к его эпителию, что является важной характеристикой потенциальных пробиотиков [35,36].
В кишечнике эти виды проявляют антибактериальные и противогрибковые свойства [35,36,37]. Также было обнаружено, что L. kefiri связывает токсичные металлы и микотоксины, что свидетельствует о его потенциале для использования в будущем в экстренной токсикологии [38,39]. L. mesenteroides может синтезировать линолевую кислоту — соединение с антиатерогенными, противовоспалительными и противораковыми свойствами [36].
L. lactis, в сравнении с ним, может производить конъюгированную линолевую кислоту, но неспособна прилипать к эпителию, что необходимо для колонизации кишечника [40,41]. Однако, несмотря на кратковременное присутствие в кишечнике, L. lactis может приносить пользу организму-хозяину, синтезируя биологические соединения с иммуномодулирующим, антибактериальным и антигипертензивным действием [41]. Именно эта особенность обеспечила L. lactis название «клеточная фабрика», а несколько исследований продемонстрировали ее потенциал в качестве средства доставки лекарственных препаратов и вакцин [42,43,44,45,46]. Другие виды МКБ, присутствующие в кефире, включают Lactobacillus acidophilus, Lactobacillus delbrueckii, Lactobacillus helveticus, Lactobacillus johnsonii, Lentilactobacillus parakefiri, Lentilactobacillus sunkii, Lacticaseibacillus rhamnosus, Lacticaseibacillus casei, Lacticaseibacillus paracasei, Lactiplantibacillus plantarum, Levilactobacillus brevis, Limosilactobacillus fermentum и Limosilactobacillus reuteri [47,48]. Однако доля и даже само наличие каждого вида бактерий в кефире варьируется в зависимости от региона, используемых субстратов и производителей [47,49,50].
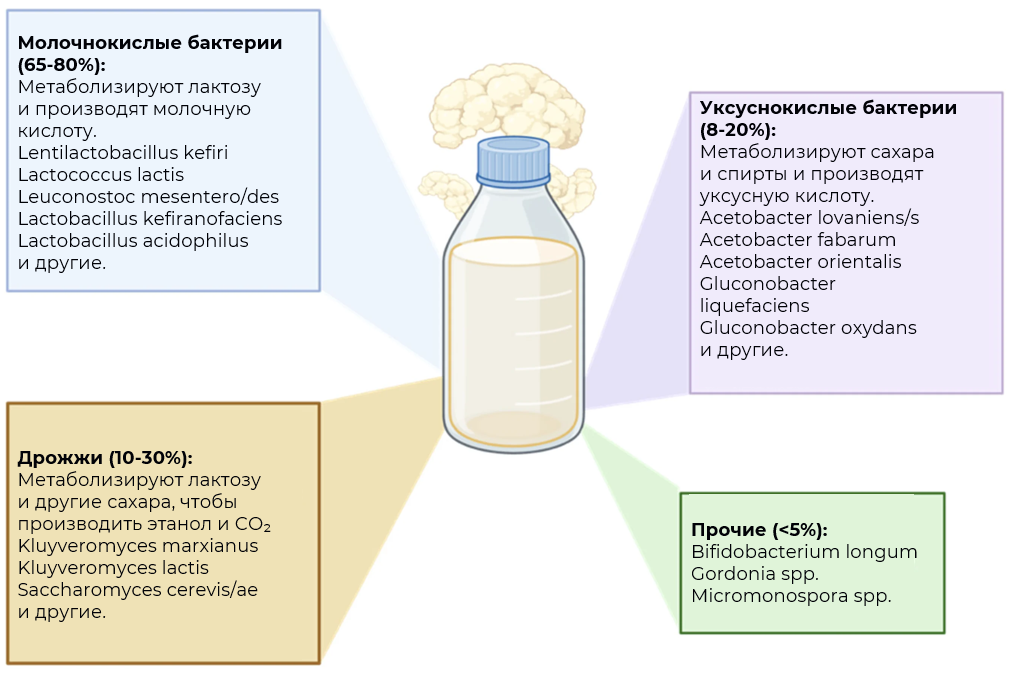 Рисунок 2. Микробный состав кефира: молочнокислые бактерии (65–80%), дрожжи (10–30%), уксуснокислые бактерии (8–20%), прочие (<5%). По El-Assaad, F. (2025).
Рисунок 2. Микробный состав кефира: молочнокислые бактерии (65–80%), дрожжи (10–30%), уксуснокислые бактерии (8–20%), прочие (<5%). По El-Assaad, F. (2025).Остальные 17–40% микроорганизмов в основном представлены уксуснокислыми бактериями (УКБ) и дрожжами [16,29,30,47]. В кефире были идентифицированы такие УКБ, как Acetobacter lovaniensis, Acetobacter fabarum, Acetobacter orientalis, Gluconobacter liquefaciens и Gluconobacter oxydans [51]. Эти бактерии, наряду с молочнокислыми, играют важную роль в ферментации кефира, производя уксусную кислоту — ключевую короткоцепочечную жирную кислоту (КЦЖК) в кишечнике [52,53,54]. Уксусная кислота и ее метаболиты оказывают локальное воздействие в виде усиления моторики подвздошной кишки и кровотока в толстой кишке, а также поддерживают гомеостаз кишечного эпителия [55,56,57]. Кроме того, недавние исследования подчеркивают ее влияние на общее состояние здоровья за счет модуляции воспалительных процессов, энергозатрат и аппетита [57].
Дрожжи включают как лактозоферментирующие виды, такие как Kluyveromyces marxianus и Kluyveromyces lactis, так и нелактозоферментирующие — Saccharomyces cerevisiae [30,58,59]. S. cerevisiae, K. marxianus и K. lactis производят этанол и углекислый газ, что придает кефиру характерный вкус и легкую газированность [60,61]. Присутствующие в кефире дрожжи, как правило, безопасны и хорошо переносятся человеческим организмом; более того, многие из них считаются пробиотиками, поскольку поддерживают иммунную функцию и здоровье кишечника [62]. В частности, S. cerevisiae var. boulardii обладает антимикробными, противораковыми, антиоксидантными и противовоспалительными свойствами [63] и, как было подтверждено, способствует уменьшению симптомов или предотвращению болезни Крона [64] и синдрома раздраженного кишечника [65].
Имеющиеся данные свидетельствуют, что S. cerevisiae может усиливать пробиотический потенциал МКБ посредством коагрегации и адгезии к эпителиальным клеткам [66], что является важным открытием с учетом общего микробиологического профиля кефира. Кефир также содержит Bifidobacterium longum, принадлежащую к семейству Bifidobacteriaceae. Хотя этот вид не является ни МКБ, ни УКБ, он известен своими пробиотическими свойствами [67,68].
Считается, что уникальное сочетание всех этих микробиологических компонентов обеспечивает разнообразие потенциальных оздоровительных эффектов кефира, включая улучшение состояния кишечника и лечение различных заболеваний [28,33,48]. Растущая популярность кефира во всем мире требует дальнейших исследований его влияния на здоровье человека. В этом обзоре рассматриваются текущие научные данные о влиянии потребления кефира на микробиом полости рта и кишечника, последствия для здоровья человека и определяются ключевые области для будущих исследований.
Методы
Был проведен поиск в базе данных PubMed и Кокрейновской библиотеке за период с января 2010 года по февраль 2025-го. Поисковые термины включали «кефир» И («микробиота кишечника» ИЛИ «микробиом кишечника» ИЛИ «микробиота полости рта» ИЛИ «микробиом полости рта» ИЛИ «слюна»). Всего было найдено 126 исследований, из которых в обзор было включено 9 [69,70,71,72,73,74,75,76,77].
Исследования включались в обзор, если они соответствовали следующим критериям: (1) рандомизированные контролируемые испытания, интервенционные исследования или исследования безопасности / возможности применения; (2) опубликованы в период с января 2010 г. по декабрь 2024 г.; (3) методы включали идентификацию кишечной или оральной микробиоты посредством экстракции и секвенирования ДНК или культивирования микроорганизмов; (4) результаты включали изменения видового разнообразия, относительной численности или количества кишечной либо оральной микробиоты. Исследования исключались, если они не были посвящены изучению человека; были обзорами, метаанализами, описаниями клинических случаев или были недоступны на английском языке. В обзор включались исследования любого вида кефира (коровьего, козьего, соевого, водного и т. д.). Большинство исследований были исключены, поскольку они не были рандомизированными контролируемыми испытаниями, интервенционными исследованиями или исследованиями безопасности и возможности применения, а также не измеряли изменения видового разнообразия, относительной численности или количества микробиоты кишечника или полости рта.
Еще одно исследование было найдено в списке литературы другого включенного в обзор исследования [78]. Было включено четыре исследования, посвященных влиянию потребления кефира на микробиом полости рта, и шесть исследований, посвященных микробиому кишечника [69,70,71,72,73,74,75,76,77,78].
Результаты
Было выявлено шесть соответствующих критериям исследований, посвященных микробиому кишечника, и четыре — посвященные микробиому полости рта (табл. 1 и табл. 2).
Обсуждение
1. Изменения микробиома кишечника, вызванные употреблением кефира
У разных групп населения потребление кефира вызывает разные изменения в микробиоме кишечника. Walsh с соавт. [72] обнаружили, что у здоровых взрослых людей, получавших кефир, увеличилось относительное количество Lactococcus raffinolactis и МКБ, присутствующих в кефирных продуктах на основе молока, но это изменение не было статистически значимым; у всех трех групп, участвующих в исследовании, не было никаких свидетельств изменения микробного разнообразия. Для сравнения, Bellikci-Koyu с соавт. [73] наблюдали значительное увеличение относительной численности Actinobacteria у лиц с метаболическим синдромом.
Yılmaz с соавт. [74] сообщили об увеличении относительной численности Lactobacillus у лиц с воспалительными заболеваниями кишечника (ВЗК). У госпитализированных пациентов в критическом состоянии Gupta с соавт. [71] отметили увеличение индекса здоровья микробиома кишечника (ИЗМК), несмотря на снижение разнообразия и количества кишечной микробиоты из-за приема антибиотиков. Напротив, Dazıroğlu с соавт. [70] обнаружили значительное увеличение микробного количества и разнообразия у женщин с синдромом поликистозных яичников (СПКЯ) после употребления кефира — возможно, из-за исключения участниц, принимавших антибиотики. Эти обобщенные данные указывают, что влияние потребления кефира на микробиом кишечника в значительной степени зависит от здоровья человека и факторов образа жизни.
Несмотря на различия в исследованиях, было получено несколько схожих результатов. В трех исследованиях была выявлена связь между повышением лабораторных показателей и улучшением показателей здоровья. Yılmaz с соавт. [74] наблюдали у лиц с ВЗК повышение уровня Lactobacillus, которое коррелировало с ослаблением желудочно-кишечных симптомов, особенно для показателей «боль в животе» и «хорошее самочувствие». Аналогичным образом, Gupta с соавт. [71] сообщили об увеличении количества Lactobacillus, что было связано с улучшением показателей ИЗМК у взрослых, находящихся в критическом состоянии. Однако это увеличение наблюдалось в течение короткого периода, всего 72 часа, во время исследования.
Dazıroğlu с соавт. [70] обнаружили у женщин с СПКЯ статистически значимое увеличение количества Bacilli, а также улучшение показателей физического и психического здоровья по сравнению с состоянием до лечения. Два исследования предоставили некоторые предварительные подтверждения того, что повышение количества МКБ может улучшить состояние здоровья, хотя четкой связи между ними установлено не было. Walsh с соавт. [72] выявили увеличение количества L. raffinolactis, хотя это наблюдалось только у четырех из десяти человек в группе, принимавшей кефир. У этих четырех участников в моче обнаружилось увеличение содержания уксусной кислоты, N,N-диметилглицина и янтарной кислоты — метаболитов, которые могут поддерживать обмен веществ, здоровье мышц и кожи [79,80,81]. Но о конкретных изменениях в состоянии здоровья этих четырех участников не сообщалось. Bellikci-Koyu с соавт. [73] у лиц с метаболическим синдромом нашли небольшое увеличение числа Lactobacillales и положительные изменения уровня инсулина натощак, TNF-α, IFN-γ и артериального давления в группе, употреблявшей кефир. Однако об изменениях общего состояния здоровья также не сообщалось. Это указывает на то, что потребление кефира, способствуя увеличению количества МКБ в кишечном микробиоме, может привести к положительным изменениям в состоянии кишечника в целом. Однако это не подтвердилось в исследовании Öneş с соавт. [69]: хотя после употребления кефира наблюдалось небольшое улучшение спортивных результатов, оно не было статистически значимым.
В рассмотренных работах сообщается об ассоциациях, а не о причинно-следственных связях, и между исследованиями, касающимися улучшения показателей здоровья, практически нет единообразия.
В трех из рассмотренных исследований сообщалось об использовании кефира разных производителей [69,71,72], в двух — о приготовлении собственного кефира с зернами от разных производителей [70,73], и в одном не сообщалось о производителе используемого кефира [74]. Стандартизированные источники кефира позволили бы провести более надежные поперечные сравнения.
Включение плацебо-контроля в дизайн исследований помогает обеспечить достоверность результатов. Однако только в одном исследовании группа, принимавшая кефир, сравнивалась с контрольной группой, получавшей плацебо [73]; в двух исследованиях была группа контроля, которая не получала никаких препаратов [69,74], а в остальных трех контрольной группы не было [70,71,72].
Кроме того, учитывая ограниченный размер выборки во всех включенных исследованиях, необходимы более масштабные испытания.
2. Изменения микробиома полости рта, вызванные употреблением кефира
Во всех исследованиях потребление кефира людьми, по-видимому, снижало численность специфических микроорганизмов полости рта. Во всех четырех исследованиях сообщалось об уменьшении количества в слюне колониеобразующих единиц (КОЕ) Streptococcus mutans — основного возбудителя кариеса — после периода употребления кефира [75,76,77,78]. Cogulu с соавт. [78] также сообщили о снижении в слюне КОЕ Lactobacillus, которые включают виды, как способствующие кариесу, так и предотвращающие его. Этот вывод отсутствовал в остальных трех исследованиях.
Общая реакция на употребление кефира в разных возрастных группах была одинаковой. Два исследования, в которых принимали участие здоровые взрослые, продемонстрировали снижение количества кариесогенных бактерий S. mutans [77,78]. В оставшихся двух исследованиях участвовали дети, проходящие ортодонтическое лечение или реставрацию зубов, и было продемонстрировано такое же снижение [75,76]. Это говорит о том, что потребление кефира может снизить численность кариесогенных бактерий независимо от возраста или состояния зубов.
Однако из-за ограниченных результатов и отсутствия долгосрочных наблюдений во всех четырех исследованиях недостаточно данных, подтверждающих, что потребление кефира напрямую снижает риск кариеса или других стоматологических заболеваний за счет изменения микробиома полости рта. Дальнейшие исследования должны включать оценку клинических результатов в ходе долгосрочного наблюдения для уточнения связи между потреблением кефира и поддержанием общего здоровья полости рта.
Хотя во всех четырех исследованиях сообщалось о снижении в слюне количества S. mutans или Lactobacillus, это были единственные наблюдаемые изменения в микробиоме полости рта. Критическим ограничением имеющихся научных данных является то, что все четыре исследования основывались исключительно на культуральных методах идентификации бактерий, присутствующих в образцах слюны. Ни в одном из четырех исследований для идентификации бактерий не использовались методы секвенирования ДНК; вместо этого применялись культивирование или тест на риск развития кариеса, который включает в себя сбор слюны пациента и использование агаровой среды для визуального определения количества S. mutans и Lactobacilli в слюне [75,76,77,78]. Поскольку эти методы являются полуколичественными и проверяют только присутствие заранее определенных бактерий, они не могут дать всестороннего представления о микробном разнообразии, а также не могут идентифицировать нестандартные и новые виды; это может быть достигнуто только с помощью секвенирования ДНК. Таким образом, использование только методов культуральной идентификации во всех четырех исследованиях в значительной степени исключает всестороннюю оценку воздействия потребления кефира на микробиологическую экологию полости рта.
Другим ограничением этих четырех исследований является использование разных кефирных продуктов. В одном исследовании для приготовления кефира использовались кефирные зерна от неустановленного производителя [77], в двух использовались разные кефирные продукты [76,78], в одном не сообщалось о производителе кефира [75].
Еще одним ограничением является относительно небольшая выборка. Только в двух исследованиях участвовало более 50 человек [76,77], причем в одном из них не сообщалось о распределении участников по группам [77]. Для обеспечения надежных результатов необходимы более масштабные эксперименты.
Кроме того, во всех исследованиях не приводилось подтверждений строгого контроля за спутывающими факторами, такими как гигиена полости рта участников и их пищевые привычки. Хотя Alp с соавт. [76] утверждают, что участники прошли обучение гигиене полости рта и им было рекомендовано чистить зубы два раза в день, подробности о характере и содержании обучения не приводились, и соблюдение участниками рекомендованных методов гигиены полости рта не фиксировалось. Reddy с соавт. [75] рекомендовали участникам соблюдать свои обычные гигиенические правила, однако нет никаких свидетельств того, что авторы контролировали соблюдение правил или корректировали их с учетом потенциальных последствий. Наконец, в двух оставшихся исследованиях не было упомянуто никаких инструкций относительно соблюдения участниками правил гигиены полости рта [77,78]. Также в этих двух исследованиях использовались интервалы в 3 недели или менее [77,78], что является более коротким периодом вмешательства по сравнению с остальными рассмотренными исследованиями микробиома кишечника и полости рта. Этого короткого периода может оказаться недостаточно для того, чтобы после употребления кефира произошли изменения в микробиоме. Таким образом, для этих двух исследований основным ограничением является короткий период наблюдения.
Заключение
В современной научной литературе указывается, что потребление кефира может влиять как на микробиом кишечника, так и на микробиом полости рта человека, но конкретный характер и масштабы этих эффектов различаются. В кишечнике кефир, по-видимому, влияет на относительное содержание Lactobacillus, а некоторые исследования показывают также улучшение самочувствия и клинических показателей. В полости рта кефир стабильно снижает уровень Streptococcus mutans, основного возбудителя кариеса; этот результат наблюдается как у взрослых, так и у детей. Однако различия в структуре исследований и показателях результатов затрудняют получение окончательных выводов о конкретных механизмах и долгосрочных клинических последствиях употребления кефира.
Будущие направления исследований
Будущие исследования должны быть направлены на преодоление многочисленных ограничений, присущих имеющимся работам. Повторяющиеся проблемы, такие как малый размер выборки, короткая продолжительность эксперимента и отсутствие надлежащего контроля, затрудняют получение достоверных данных. Различия в производителях кефирных зерен или кефира могут приводить к появлению дополнительных спутывающих факторов, влияющих на результаты экспериментов. В исследованиях микробиома полости рта использование культуральных методов и тестов на риск развития кариеса вместо методов следующего поколения (секвенирования ДНК) ограничивает масштаб исследования только оценкой изменений количества заранее выбранных бактерий; в результате изменения альфа-/бета-разнообразия и относительной численности не оцениваются.
Будущие исследования должны устранить эти пробелы за счет более масштабных и хорошо контролируемых экспериментов с подбором участников по возрасту, полу и этнической принадлежности, с использованием стандартизированных кефирных продуктов, хорошо изученных субстратов для получения кефира (молочных или растительных) и всестороннего анализа микробиома. Кроме того, необходимы более длительные исследования для оценки долгосрочного воздействия кефира на клинические исходы, включая частоту возникновения кариеса и профилактику или лечение кишечных расстройств. Устранение перечисленных выше ограничений позволит получить более полное представление о пользе кефира для здоровья и его терапевтическом потенциале.














