Почему мышца растет в ответ на физические упражнения

Мышечная ткань – одна из немногих, способных как увеличиваться, так и уменьшаться в размерах в течение жизни. Исследования на людях и животных показывают, что ключом к росту мышц служат повторяющиеся высокоинтенсивные упражнения, однако механизмы, регулирующие этот рост, пока не вполне ясны. Специалисты Лондонского Королевского колледжа Майкл Аттуотерс и Саймон Хьюз проанализировали публикации, посвященные факторам, воздействующим на работающие скелетные мышцы.
У взрослых людей большинство клеток сохраняют постоянный размер, при этом некоторые из них могут делиться. Однако зрелые скелетные мышечные волокна не делятся, но растут. Они увеличиваются в размерах в результате физической нагрузки, отчего растет и объем мышц. Атлеты целенаправленно его увеличивают силовыми упражнениями. Напротив, в периоды бездействия, например, при постельном режиме или в условиях невесомости мышечные волокна атрофируются.
Скелетные мышцы могут расти тремя способами. Рост в результате образования новых мышечных волокон (режим 1) происходит в основном внутриутробно. Позже мышца растет в результате добавления новых ядер к уже имеющимся мышечным волокнам (режим 2). Рост ранее существовавших волокон также происходит за счет увеличения размера ядерного домена (режим 3). При атрофии размер ядерного домена уменьшается.
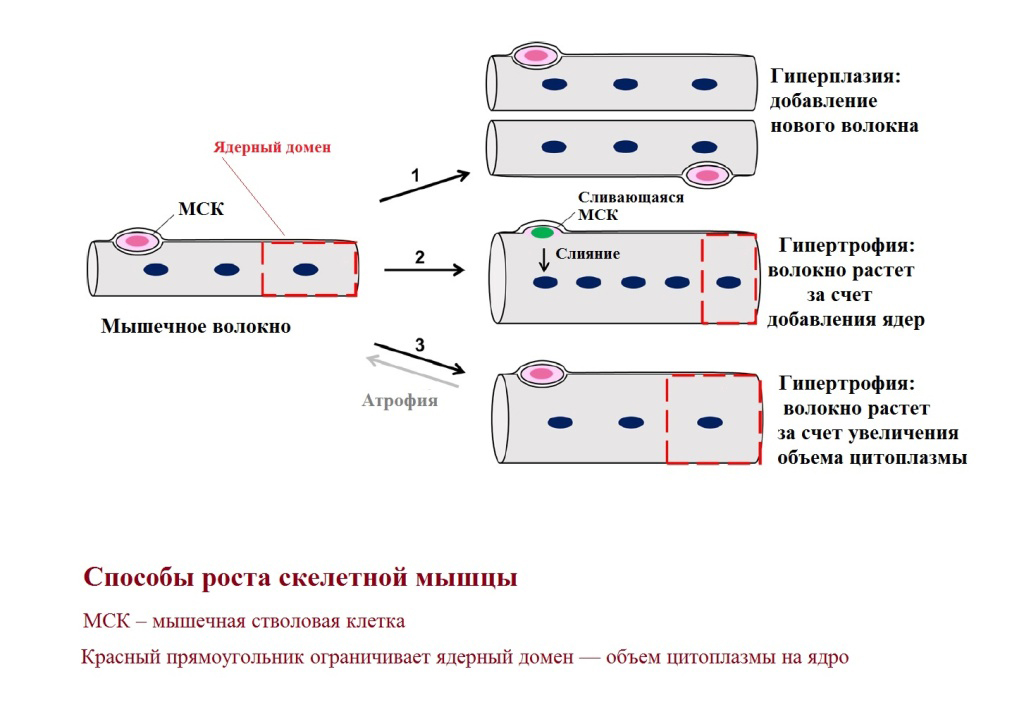
Каждое мышечное волокно представляет собой синцитий, образованный слиянием клеток-предшественников. Синцитий — это несколько клеток, соединенных цитоплазматическими мостиками. При гипертрофии объем волокна увеличивается за счет увеличения объема цитоплазмы или количества ядер, поскольку каждое ядро может поддерживать конечный максимальный объем цитоплазмы. Дополнительные ядра появляются в результате слияния с мышечными стволовыми клетками (МСК). Слияние происходит после тренировки, что подтверждается экспериментально. Однако гипертрофия может происходить и без слияния клеток.
Системный контроль роста скелетных мышц
Рост мышц находится под двойным контролем: системным и локальным. Системный контроль осуществляют циркулирующие гормоны и питательные вещества. Примером такого системного контроля может служить голодание, когда мышцам приходится отдавать аминокислоты для синтеза глюкозы в печени и почках, в конечном итоге обеспечивая питание жизненно важных органов. Мышцы в результате истощаются. Правильное питание способствует поддержанию мышечной массы у пожилых людей, смягчая саркопению.
Для мышечного роста необходим активный синтез белка, который находится под контролем гормонов: тестостерона, инсулина и инсулиноподобного фактора роста 1 (ИФР-1), миостатина, глюкагона и бета-адренергического сигнального пути.
Лучше всего изучено действие ИФР-1 и миостатина. При усиленном синтезе ИФР-1 происходит гипертрофия скелетных мышц и увеличение их силы. Миостатин — негативный регулятор мышечной массы. Его избыток приводит к атрофии скелетных мышц, а ингибирование — к гипертрофии мышечной ткани.
Разные мышцы по-разному реагируют на один и тот же сигнал, например, на отсутствие миостатина. Одно из возможных объяснений заключается в том, что решающее значение имеют местные механизмы регуляции. Эту точку зрения подтверждает тот факт, что при физических упражнениях растут только тренируемые мышцы, несмотря на значительное повышение уровня системных гормонов. Циркулирующие гормоны могут разрешать рост мышц, но не стимулировать его в обязательном порядке. Так, для локальной мышечной гипертрофии в ответ на перегрузку необходим минимальный базальный уровень тестостерона. Общий гормональный статус организма может влиять на чувствительность мышцы к локальным сигналам. Что же это за сигналы?
Электрический импульс и ионы кальция
Мышечное сокращение начинается с возбуждения двигательного нерва, то есть с электрического импульса. Он вполне может быть триггером мышечной гипертрофии. Еще в 1974 году было показано, что прямая электрическая стимуляция денервированных мышц восстанавливает мышечную массу. Для этого нерв не нужен, нужна только электрическая активность. Кроме того, эти импульсы влияют на другие процессы, происходящие в возбужденном мышечном волокне: секрецию сигнальных молекул и выделение ионов кальция.
У ионов Са2+ множество функций. В скелетных мышцах они регулируют деление миобластов, апоптоз, дифференцировку волокон и их сокращение. В условиях покоя концентрация Ca2+ в цитоплазме одного мышечного волокна составляет 30–50 нМ. При каждой деполяризации мембраны высвобождается кальций, накопленный в саркоплазматическом ретикулуме (это специальная мембранная органелла мышечных клеток, служащая для запасания Са2+), а также некоторое его количество поступает в клетку из внеклеточного пространства. В результате концентрация свободного Ca2+ в саркоплазме возрастает примерно в сто раз, он связывается с тропонином С и активирует актомиозиновое сокращение.
Помимо непосредственного руководства мышечным сокращением, кальций регулирует сигнальные пути, ответственные за поддержание фенотипов быстрых и медленных мышечных волокон. И поскольку он взаимодействует с другими факторами, влияет, в частности, на активацию разных ферментов и транспорт глюкозы, выделить его роль в гипертрофии мышц сложно. Пока нельзя сказать, достаточно ли одного Са2+ для индукции мышечного роста или важны и другие факторы.
Концентрация ионов кальция при активных сокращениях возрастает ненадолго, от нескольких секунд до минут. Когда сокращения прекращаются, Ca2+ быстро возвращается к исходному уровню. Однако за эти нескольких минут кальций успевает запустить работу генов, необходимых для мышечной гипертрофии. Работают эти гены довольно долго, даже после того, как концентрация Ca2+ снизилась.
Энергетический стресс и метаболическая гипотеза
Активация мышц сопряжена с огромными энергетическими затратами, при этом скорость оборота АТФ во время упражнений с максимальной нагрузкой увеличивается в сто раз. Мышечное волокно располагает некоторым запасом АТФ, но он истощается за несколько секунд, и клетка использует для регенерации АТФ и поддержания запаса энергии фосфат, гликоген и липиды. Этому сопутствуют метаболические изменения, в том числе увеличение концентрации АМФ и других веществ, которые могут служить триггерами гипертрофии.
Возможно, в роли триггеров выступают лактат и реактивные формы кислорода (АФК). Анаболические свойства лактата доказаны экспериментально. У животных он ускорял регенерацию поврежденных мышц и стимулировал мышечную гипертрофию даже в отсутствие упражнений. Косвенно роль лактата подтверждают результаты упражнений, выполняемых с наложением жгутов. Ограничение кровотока вызывает местную гипоксию, а побочные продукты метаболизма плохо удаляются через венозный кровоток и накапливаются. Показано, что ограничение кровотока увеличивает гипертрофию мышц в ответ на физические упражнения с низкой нагрузкой (ходьбу), вероятно, в результате увеличения концентрации метаболитов или локальной гипоксии.
Одна из проблем, связанных с этой гипотезой, заключается в том, что мы пока не знаем, как клетка может почувствовать лактат. Другие соединения, которые действовали на животных как анаболики, — фосфатидная кислота и оксид азота.
Возможно, метаболиты контролируют рост мышц косвенным образом. Накопленный лактат подкисляет внутримышечную среду и стимулирует метаборецепторы (это рецепторы скелетных мышц, которые реагируют на увеличение концентрации метаболитов и стимулируют увеличение кровообращения в ответ на упражнение), а также афферентные волокна III и IV групп. В результате ингибируется активность альфа-мотонейронов и, чтобы компенсировать ослабление их функции, увеличивается количество работающих нейронов. Эта гипотеза подтверждается тем, что упражнения с низкой нагрузкой в сочетании с ограниченным кровообращением увеличивают амплитуду электромиографии целевой мышцы.
Следовательно, метаболические стрессоры активируют большую часть мышечных волокон косвенным образом, увеличивая нервно-мышечную активацию, что способствует гипертрофии целой мышцы. Но эта гипотеза еще нуждается в тщательной проверке.
Механические сигналы
На форму и размер тканей взрослого человека влияет четко скоординированное взаимодействие механических и биохимических стимулов. Особенно это влияние ощущается в костно-мышечной системе. Примером может служить более крупный размер кости в ведущей руке теннисистов, вызванный механическими нагрузками при повторяющихся ударах. В литературе преобладает гипотеза, согласно которой механические сигналы воспринимаются мышечными волокнами и преобразуются в биохимические сигналы, регулирующие работу соответствующих генов.
Механические стимулы бывают разные. Один из вариантов — растяжение мышц. В литературе было несколько сообщений о том, что иммобилизационное растяжение мышц у животных вызывает их гипертрофию. В некоторых работах сообщалось, что этот эффект носит временный характер, и мышцы в конечном итоге атрофируются. Однако совокупные данные из нескольких лабораторий показали, что растяжение мышц крыльев птиц приводит к выраженной мышечной гипертрофии. Все эти исследования выполнены в прошлом веке.
Тем не менее следует учесть, что растянутые мышцы более неврологически активны, чем укороченные, поэтому некоторый рост может быть вызван электрической активностью волокон, а не механическими усилиями. Кроме того, хроническое растяжение сильно отличается от прерывистых упражнений, выполняемых во время тренировок с отягощениями, и потому имеет сомнительную экологическую значимость.
У растяжения и сокращения разный эффект. Поскольку кости во время развития удлиняются, растяжение явно увеличивает мышечную массу за счет добавления ядер и саркомеров на концах волокон, а тренировка увеличивает ширину волокон. Чтобы при пассивном растяжении вызвать воздействие, сопоставимое с напряжением, возникающим при активном сокращении, мышца должна быть растянута за пределы физиологически значимого расстояния. Кроме того, рост мышц может происходить в ответ на изометрические сокращения, при которых длина мышцы не изменяется. Все эти соображения следует учитывать, обсуждая растяжку как стимул роста мышц.
То ли дело сила! Когда мышцы крыс подвергали разной механической нагрузке, то оказалось, что изометрические сокращения с высокими нагрузками позволяют достичь вдвое большей гипертрофии мышц, чем высокоскоростные концентрические сокращения с 50–60% пиковой силы, создаваемой в группе повышенной нагрузки. Исследователи пришли к выводу, что сила мышечного сокращения действительно служит ключевым аспектом гипертрофии мышечных волокон, хотя найти сигнальные механизмы мышечного роста им не удалось.
Сенсорами, воспринимающими силу и передающими механические сигналы, могут быть, например, трансмембранные белки интегрины, которые связывают клетку с внеклеточным матриксом. Известно, что усиленная экспрессия интегрина защищает клеточную мембрану мышечного волокна от повреждений, вызванных физической нагрузкой. В клетке есть несколько молекул, взаимодействующих с интегрином и могущих повлиять на работу ключевых генов, ответственных за белковый синтез.
Механосенсоры расположены не только на мышечной мембране. Эту функцию может выполнять гигантский белок поперечно-полосатых мышц титин, взаимодействующий со многими другими белками, или мышечный белок LIM, расположенный в Z-диске. У мышей, лишенных LIM, регенерация поврежденных скелетных мышц происходит с задержкой.
Сигнальные пути
И системные, и локальные сигналы, очевидно, влияют на работу многих генов. Речь идет о сигнальных каскадах: стимул влияет на один какой-нибудь фактор, тот, в свою очередь, на несколько других, и вот уже мышца растет. Одним из ключевых регуляторов клеточного роста считают ген ТORC1. Его работа необходима для мышечной гипертрофии, вызванной физическими упражнениями. Но существуют и пути регуляции, независимые от TOR и не менее важные. Один из них — активация митоген-активированной протеинкиназы (MAPK) в ответ на физическую нагрузку. Нагрузка запускает каскад реакций, которые приводят к активации фермента и, в свою очередь, активации гена JNK, который участвует в гипертрофии мышц. По-видимому, гипертрофии способствует координация работы ТORC1и JNK.
Еще одна возможность — сигнальный путь Hippo, который активируется в ответ на механическое возбуждение. Увы, пока неясно, как эти многочисленные внутриклеточные сигнальные пути взаимодействуют в общей схеме контроля размера мышцы. Кроме того, относительная роль локальных триггеров гипертрофии: электрического сигнала, изменения концентрации ионов кальция и энергетических метаболитов, механических стимулов, также нуждается в уточнении.
По мнению Майкла Аттуотерса и Саймона Хьюза, задача ученых состоит в том, чтобы разобраться в хитросплетении всех этих триггеров роста и сигнальных путей и научиться контролировать гипертрофию мышечного волокна. Понимание механизмов роста мышц имеет решающее значение для предотвращения возрастной потери мышечной массы, сердечно-сосудистых заболеваний, кахексии и других недугов, поражающих мышцы.